En tant qu'entreprise spécialisée dans la modification des plastiques, nous ne pouvons pas simplement considérer le talc comme une charge bon marché permettant de réduire les coûts. D'un point de vue physico-chimique et cristallographique, le talc est un minéral fonctionnel doté d'une géométrie microscopique unique, d'une chimie de surface complexe et d'effets de nucléation. Ci-dessous, je dépasserai la notion générale d'augmentation de la rigidité et de réduction des coûts pour proposer une analyse approfondie de l'essence structurale et du mécanisme de modification du talc.
Structure cristalline et forces intercouches : pourquoi possède-t-elle une lubrification naturelle ?
La structure moléculaire en sandwich du talc pur a pour formule chimique Mg₃Si₄O₁₀(OH)₂. Cristallographiquement, elle est constituée de deux couches tétraédriques de siloxane (Si₂O₅) enserrant une couche octaédrique de brucite (Mg(OH)₂). Cette structure est chimiquement et électriquement neutre. (Les paillettes de mica sont chargées électriquement.)
Contrairement au mica (qui repose sur des liaisons ioniques) ou au kaolin (qui repose sur des liaisons hydrogène), les forces intercouches du talc sont maintenues ensemble par des forces de van der Waals extrêmement faibles entre les couches adjacentes.
Rôle clé des forces intercouches : Cette faible force est la raison fondamentale pour laquelle le talc est le minéral le plus tendre de la nature (dureté Mohs 1). Sous l’effet des fortes forces de cisaillement de l’extrusion et du moulage par injection de plastique, le talc s’exfolie facilement (séparation des lamelles), ce qui lui confère non seulement un excellent pouvoir lubrifiant, réduisant ainsi l’usure des vis et des moules, mais permet également la formation in situ de micro-paillettes à rapport d’aspect élevé (5:1 à 20:1) lors de la transformation.
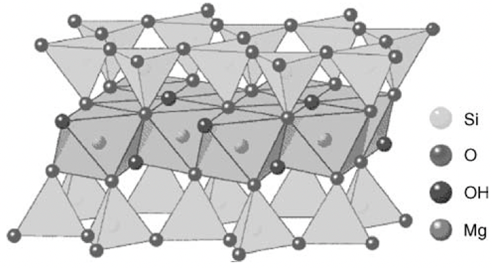
2. Groupes de surface et propriétés chimiques : L’énorme différence entre la base et les bords
La chimie de surface du talc présente une anisotropie extrêmement forte, ce qui est crucial pour le succès de sa modification de surface :
La surface basale représente la quasi-totalité de la surface totale. Du fait de sa structure exposée, constituée d'un réseau de siloxane (Si-O-Si) dépourvu de groupements polaires isolés, elle ne peut former de liaisons hydrogène avec l'eau. Par conséquent, la surface basale du talc est naturellement hydrophobe et très inerte (contrairement à la plupart des minéraux qui sont hydrophiles).
Les bords de la fracture n'occupent qu'une très petite surface. Au niveau de la fracture par meulage, des sites actifs extrêmement complexes sont exposés, notamment : des groupes silanol terminaux faiblement acides (HO-Si), des groupes hydroxyle de magnésium faiblement basiques (Mg(OH)₂), des sites de Brønsted fortement acides et des sites acides de Lewis. (Ces sites sont très importants.)
À des valeurs de pH de 8,5 à 10,7, les bords de fracture du cristal exposent des sites structuraux de brucite faiblement basiques, aggravés par des impuretés alcalines naturelles telles que le carbonate de magnésium dans le minerai.
L'hydrophobicité naturelle du talc modifié facilite sa dispersion dans les polymères non polaires (comme le PP) par rapport aux autres silicates. Cependant, comme ses groupes hydroxyle réactifs sont presque entièrement confinés à ses bords, le talc est extrêmement insensible aux agents de couplage silane traditionnels (contrairement à la silice et au GF qui y sont extrêmement sensibles).

